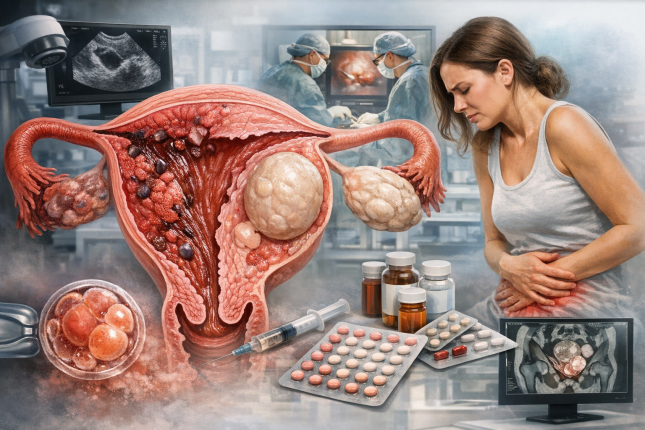
Аденоміоз і міома матки традиційно розглядаються як окремі нозології, однак сучасні дані свідчать про їхню складну біологічну взаємодію, спільні молекулярні механізми та значний вплив на репродуктивне здоров’я жінки. Останні публікації у фахових виданнях, зокрема в журналі Human Reproduction, акцентують на переосмисленні патогенезу, фенотипічної гетерогенності аденоміозу та нових підходах до стратифікації ризиків і вибору терапії.
Аденоміоз як системне, а не лише «локальне» захворювання міометрія
Сучасне бачення аденоміозу виходить за межі класичної концепції «інвагінації базального ендометрія в міометрій». У фокусі — дисфункція зони з’єднання (junctional zone), хронічне стерильне запалення, нейроангіогенез і порушення тканинної архітектоніки. Дані морфологічних та молекулярних досліджень свідчать, що аденоміоз є естроген-залежним, прогестерон-резистентним станом із вираженою локальною ароматазною активністю та зміненим профілем цитокінів.
Окрему увагу приділяють фенотипам аденоміозу — дифузному, вузловому та змішаному. Фенотипічна класифікація має не лише описове, а й прогностичне значення: глибина інфільтрації, залучення зони з’єднання та асоціація з ендометріозом впливають на вираженість болю, ризик аномальних маткових кровотеч і репродуктивні наслідки.
Підкреслюється також тісний зв’язок аденоміозу з ендометріозом як частини єдиного континууму «ендометріоз-асоційованих» захворювань. Це змушує розглядати пацієнтку не ізольовано в межах однієї патології, а в ширшому контексті системної гормонально-імунної дисрегуляції.
Міома матки: гетерогенність, прогресія та ризик помилкової «стабільності»
Міома матки залишається найпоширенішою доброякісною пухлиною жіночої репродуктивної системи. Проте сучасні публікації наголошують: не всі лейоміоми є біологічно однаковими. Генетична гетерогенність (зокрема мутації MED12 та інші молекулярні підтипи) визначає темп росту, чутливість до гормональної терапії та ризик рецидиву після органозберігаючих втручань.
Окремий інтерес викликають дані щодо поєднання міоми та аденоміозу. Так званий «adenomyosis–fibroid complex» асоціюється з тяжчими менорагіями, більш вираженим больовим синдромом та нижчими показниками успішності програм ДРТ. У таких пацієнток ізольоване лікування лише міоми (наприклад, міомектомія) не завжди забезпечує очікуваний клінічний ефект через недооцінений внесок аденоміозу.
Репродуктивні наслідки: що змінилося у розумінні
Нові клінічні дані свідчать, що аденоміоз асоціюється зі зниженням імплантаційного потенціалу, підвищенням частоти ранніх репродуктивних втрат, передчасних пологів і акушерських ускладнень. Порушення перистальтики матки, зміни експресії рецепторів до прогестерону та локальне запалення розглядаються як ключові механізми імплантаційної дисфункції.
У пацієнток із міомою значущими залишаються розмір, локалізація та деформація порожнини матки. Проте сучасний підхід дедалі більше враховує не лише механічний фактор, а й зміни мікрооточення ендометрія.
Таким чином, планування вагітності потребує індивідуалізованої стратегії. Вибір між консервативною гормональною терапією, хірургічним лікуванням або очікувальною тактикою має базуватися на поєднанні клінічних, ультразвукових та репродуктивних параметрів.
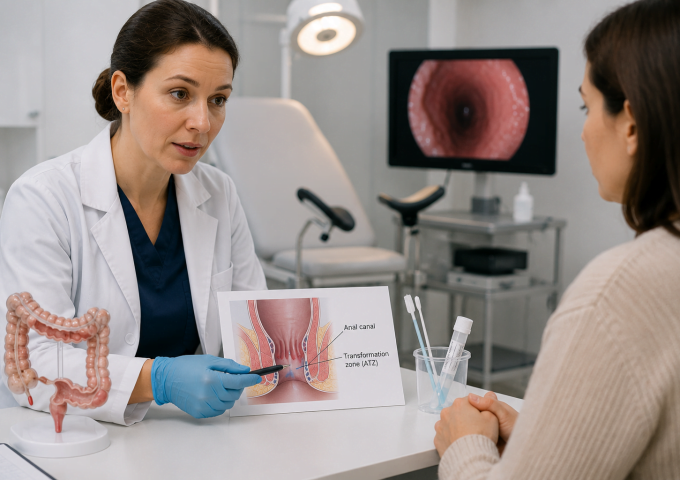
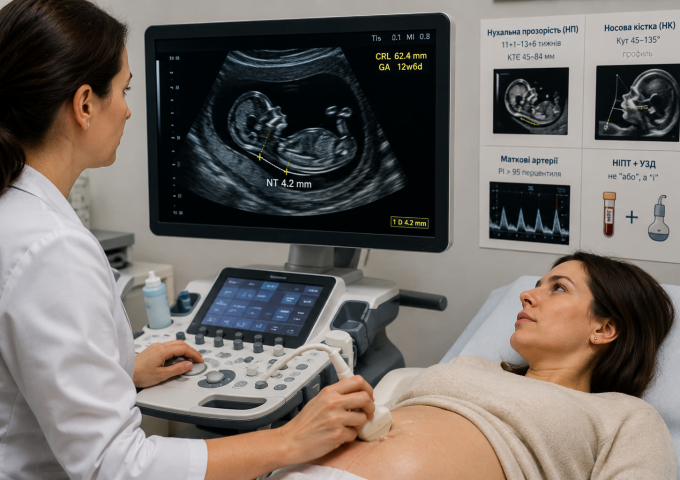
Діагностика: роль високоточної візуалізації
Трансвагінальне УЗД із оцінкою зони з’єднання залишається методом першої лінії. Для аденоміозу характерними є асиметрія стінок матки, міометріальні кісти, нечіткість межі ендометрій–міометрій, гіпоехогенні ділянки без чіткої капсули. Доплерометрія дозволяє оцінити судинний патерн, що має значення в диференційній діагностиці з вузловими формами міоми.
МРТ зберігає роль «золотого стандарту» у складних випадках, особливо перед плануванням оперативного втручання чи ДРТ. Товщина та нерівність junctional zone мають прогностичну цінність щодо симптоматики та репродуктивних результатів.
Консервативна терапія: рух до персоналізації
Серед медикаментозних підходів зберігають значення прогестини, комбіновані гормональні контрацептиви, агоністи та антагоністи ГнРГ. Водночас акцент зміщується з «тимчасового контролю симптомів» до довгострокового менеджменту з урахуванням віку, репродуктивних планів і фенотипу захворювання.
Антагоністи ГнРГ нового покоління з add-back терапією розглядаються як перспективний інструмент у пацієнток із симптомною міомою та поєднаним аденоміозом. Однак довгострокові дані щодо впливу на фертильність та рецидиви ще накопичуються.
Хірургічне лікування: баланс між радикальністю та збереженням функції
Гістероскопічна резекція підслизових вузлів, лапароскопічна міомектомія та аденоміомектомія залишаються ключовими органозберігаючими методами. Проте сучасні рекомендації наголошують: при поєднаній патології результат залежить від повноти передопераційної діагностики.
Супрацервікальна або тотальна гістеректомія розглядаються як метод вибору у пацієнток із завершеною репродуктивною функцією та тяжкою симптоматикою. Водночас зростає інтерес до менш інвазивних підходів, зокрема емболізації маткових артерій, хоча при аденоміозі її ефективність є менш передбачуваною.
Клінічні виклики та напрямки майбутніх досліджень
Головний виклик — відсутність уніфікованої класифікації аденоміозу та стандартизованих критеріїв оцінки відповіді на лікування. Сучасні дослідження спрямовані на пошук біомаркерів прогресії, предикторів відповіді на гормональну терапію та оптимального часу для хірургічного втручання перед плануванням вагітності.
У фокусі — концепція персоналізованої гінекології, де рішення приймається не лише на основі розміру вузла чи товщини міометрія, а з урахуванням молекулярного профілю, фенотипу, больового синдрому та репродуктивних намірів пацієнтки.
Сучасний підхід до міоми матки та аденоміозу — це відхід від алгоритму «одна хвороба — одне рішення» до багатовимірної клінічної моделі. Саме така стратегія дозволяє досягти оптимального контролю симптомів, мінімізувати ускладнення та зберегти репродуктивний потенціал жінки.
Категорії
Позначки
Вас також може зацікавити
-
-
04.06.2026
-
-
03.06.2026
-
-
02.06.2026